9月6日,石藥集團(tuán)發(fā)布公告稱,附屬公司上海津曼特生物科技開發(fā)的1類新藥納魯索拜單抗注射液獲批上市,用于治療不可手術(shù)切除或手術(shù)切除可能導(dǎo)致嚴(yán)重功能障礙的骨巨細(xì)胞瘤。近幾年,石藥集團(tuán)猛攻1類新藥,今年以來已有兩款1類新藥報(bào)產(chǎn)在審。

公告中提到,納魯索拜單抗注射液為全球首個(gè)獲批上市的IgG4亞型全人源抗RANKL單克隆抗體,目前同靶點(diǎn)已上市藥物地舒單抗為IgG2亞型,與地舒單抗相比,該新藥的均一性、質(zhì)量可控性均得到顯著提升。
圖1:地舒單抗的國(guó)內(nèi)銷售情況(單位:萬元)
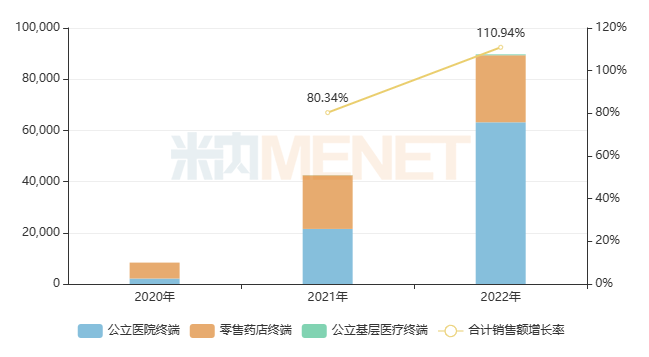
來源:米內(nèi)網(wǎng)格局?jǐn)?shù)據(jù)庫(kù)
安進(jìn)的地舒單抗在2019年獲批進(jìn)入中國(guó)市場(chǎng),2020年進(jìn)入國(guó)家醫(yī)保談判目錄,現(xiàn)為2022版國(guó)家醫(yī)保談判目錄乙類品種,限絕經(jīng)后婦女的重度骨質(zhì)疏松以及不可手術(shù)切除或者手術(shù)切除可能導(dǎo)致嚴(yán)重功能障礙的骨巨細(xì)胞瘤。
在醫(yī)保的助力下,該產(chǎn)品在中國(guó)三大終端六大市場(chǎng)(統(tǒng)計(jì)范圍見文末)的合計(jì)銷售額持續(xù)高漲,2022年合計(jì)銷售額已超過8億元,增長(zhǎng)率達(dá)110.94%,潛力可期。
圖2:納魯索拜單抗注射液開展臨床的適應(yīng)癥情況
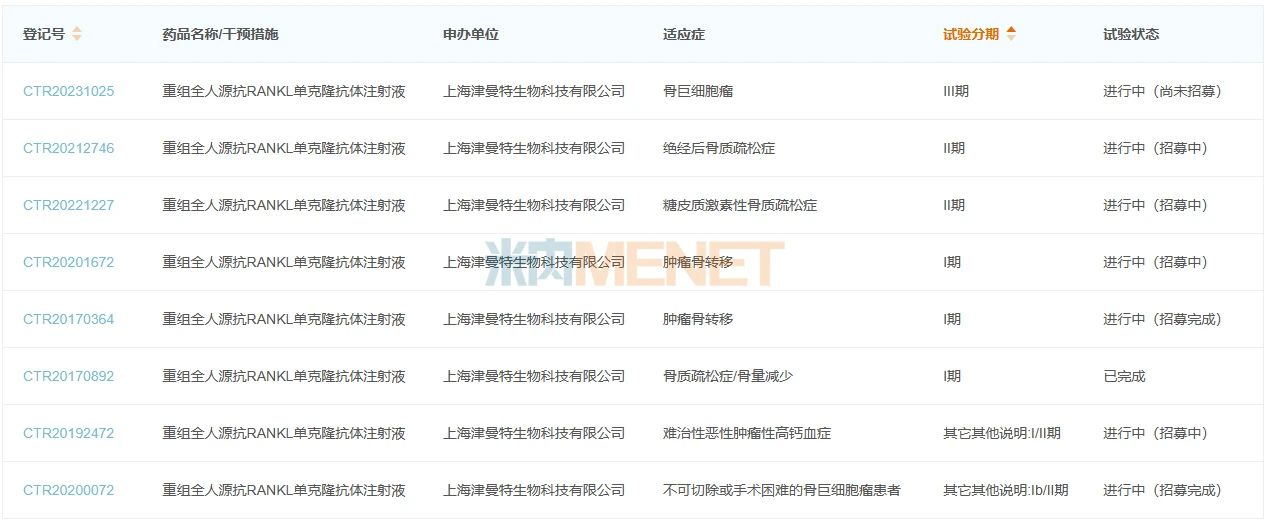
來源:米內(nèi)網(wǎng)中國(guó)臨床試驗(yàn)數(shù)據(jù)庫(kù)
本次納魯索拜單抗注射液獲批上市的適應(yīng)為用于治療不可手術(shù)切除或手術(shù)切除可能導(dǎo)致嚴(yán)重功能障礙的骨巨細(xì)胞瘤成人患者,據(jù)石藥集團(tuán)表示,目前該新藥正在開發(fā)的其他適應(yīng)癥還包括腫瘤骨轉(zhuǎn)移和骨質(zhì)疏松癥等。
表1:今年以來石藥集團(tuán)申報(bào)上市的1類新藥
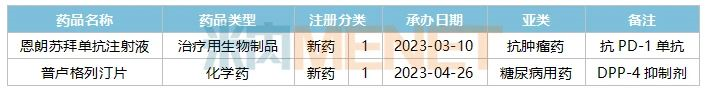
來源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫(kù)
米內(nèi)網(wǎng)數(shù)據(jù)顯示,今年以來石藥集團(tuán)提交了兩款1類新藥的上市申請(qǐng),目前正在審評(píng)審批中。恩朗蘇拜單抗注射液是一款重組抗PD-1全人源單克隆抗體,屬IgG4型單抗藥物,用于治療至少一線含鉑方案化療失敗的PD-L1表達(dá)陽(yáng)性的復(fù)發(fā)或轉(zhuǎn)移性宮頸癌患者。普盧格列汀片是一種新型DPP-4抑制劑,用于治療2型糖尿病。
資料來源:公司公告、米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)
注:米內(nèi)網(wǎng)《中國(guó)三大終端六大市場(chǎng)藥品競(jìng)爭(zhēng)格局》,統(tǒng)計(jì)范圍是:城市公立醫(yī)院和縣級(jí)公立醫(yī)院、城市社區(qū)中心和鄉(xiāng)鎮(zhèn)衛(wèi)生院、城市實(shí)體藥店和網(wǎng)上藥店,不含民營(yíng)醫(yī)院、私人診所、村衛(wèi)生室,不含縣鄉(xiāng)村藥店;上述銷售額以產(chǎn)品在終端的平均零售價(jià)計(jì)算。數(shù)據(jù)統(tǒng)計(jì)截至9月7日。

