隨著《2022年國家基本醫(yī)療保險(xiǎn)、工傷保險(xiǎn)和生育保險(xiǎn)藥品目錄調(diào)整工作方案》(簡稱《方案》)正式公布,7月份以來,第五輪國家醫(yī)保藥品目錄調(diào)整工作正式進(jìn)入企業(yè)品種申報(bào)階段。
自2018年國家醫(yī)保局正式成立后,醫(yī)保目錄調(diào)整工作開始進(jìn)入常態(tài)化,醫(yī)保目錄調(diào)整規(guī)則也得到不斷完善:
2019年,醫(yī)保目錄調(diào)整工作方案明確調(diào)入分為常規(guī)準(zhǔn)入和談判準(zhǔn)入兩種方式,目錄新增“協(xié)議期內(nèi)談判藥品”類別。
2020年,醫(yī)保目錄調(diào)整正式啟動(dòng)企業(yè)自主申報(bào)機(jī)制,明確國家醫(yī)療保障經(jīng)辦機(jī)構(gòu)將按規(guī)定組織藥物經(jīng)濟(jì)學(xué)、醫(yī)保管理等方面專家開展談判或準(zhǔn)入競價(jià)。
2021年,醫(yī)保目錄調(diào)整規(guī)則基本成熟,進(jìn)一步凸顯藥品臨床綜合評(píng)價(jià)及藥物經(jīng)濟(jì)學(xué)在醫(yī)保談判中的作用。
今年,正式發(fā)布的《方案》在藥品目錄調(diào)整工作程序方面增加了更多的細(xì)節(jié),不僅要求申報(bào)內(nèi)容需要提交申報(bào)資料和摘要幻燈片,并首次對(duì)外公開《談判藥品續(xù)約規(guī)則》《非獨(dú)家藥品競價(jià)規(guī)則》等文件。
市場普遍認(rèn)為,醫(yī)保談判的關(guān)注點(diǎn)已經(jīng)不只是降低藥品價(jià)格,新一輪醫(yī)保目錄調(diào)整工作,更傾向通過完善制度建設(shè)規(guī)范價(jià)格體系;同時(shí),綜合考慮2021年通過形式審查、未進(jìn)入醫(yī)保的新通用名藥品,2022年獲批的新通用名藥物,醫(yī)保目錄內(nèi)獲批新適應(yīng)癥藥品,目錄內(nèi)品種到期等情況,本次醫(yī)保談判結(jié)果依然值得期待。
01、合理競爭規(guī)范價(jià)格 鼓勵(lì)產(chǎn)品橫向?qū)Ρ?/strong>
和往年一樣,今年的醫(yī)保談判工作仍分為準(zhǔn)備、申報(bào)、專家評(píng)審、談判/競價(jià)、公布結(jié)果5個(gè)階段。根據(jù)方案規(guī)劃的時(shí)間點(diǎn),目前正是企業(yè)準(zhǔn)備申報(bào)信息資料并進(jìn)行網(wǎng)上申報(bào)的關(guān)鍵階段。
據(jù)悉,在申報(bào)準(zhǔn)備方面,與往年相比,今年最大的不同是申報(bào)企業(yè)需要在7月14日17:00前提交申報(bào)材料和摘要幻燈片(PPT),明確填寫基本信息、安全性、有效性、經(jīng)濟(jì)性、創(chuàng)新性和公平性,其中很多內(nèi)容不僅關(guān)系到企業(yè)的降價(jià)依據(jù),而且可能涉及產(chǎn)品間的橫向?qū)Ρ燃搬t(yī)保方價(jià)格測算。
按照規(guī)則,國家醫(yī)保局要求企業(yè)在PPT填上申報(bào)品種的基本信息,從2020年1月1日至2022年6月30日在中國大陸地區(qū)的銷售金額,主要?jiǎng)?chuàng)新點(diǎn)等;此外,規(guī)則要求企業(yè)提交“同治療領(lǐng)域藥品”“同通用名藥品”的上市情況、經(jīng)濟(jì)性、臨床價(jià)值等對(duì)比信息。
行業(yè)專家認(rèn)為,這一舉措無異于通過企業(yè)之間的申報(bào)資料互相佐證甚至相互“曝光”,讓企業(yè)在相同治療領(lǐng)域、相同適應(yīng)癥之間競爭,或許將加劇產(chǎn)品和治療方案之間的價(jià)格博弈。

同時(shí),為了防止“串標(biāo)”“圍標(biāo)”等行為,政策也進(jìn)一步限定企業(yè)合規(guī)競價(jià)行為 。

國家醫(yī)保局還特別規(guī)定:禁止在申報(bào)材料中,出現(xiàn)國家機(jī)關(guān)、學(xué)術(shù)機(jī)構(gòu)、行業(yè)協(xié)會(huì)或者領(lǐng)導(dǎo)、醫(yī)師、患者及其他人員的姓名、照片、圖像等,以及其他誤導(dǎo)性、誘導(dǎo)性、夸大性內(nèi)容。并在最后一條要求中強(qiáng)調(diào)“如有不符不予采用”,進(jìn)一步強(qiáng)調(diào)公平競爭。
為進(jìn)一步加大企業(yè)競爭,《非獨(dú)家藥品競價(jià)規(guī)則》對(duì)于非獨(dú)家品種的醫(yī)保準(zhǔn)入制度設(shè)計(jì)做出了調(diào)整,有助于改變以往臨床價(jià)格高昂的非獨(dú)家品種缺乏合理的準(zhǔn)入機(jī)制的問題。
2020年7月30日,國家醫(yī)保局發(fā)布《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》,規(guī)定除帶量采購中選藥品外,其他非獨(dú)家藥品根據(jù)準(zhǔn)入競價(jià)等方式確定支付標(biāo)準(zhǔn)。不過,非獨(dú)家藥品采用競價(jià)方式準(zhǔn)入,并沒有在此前的醫(yī)保談判中落地。
此次醫(yī)保談判的非獨(dú)家藥品競價(jià)規(guī)則主要是:
醫(yī)保方測算并提出醫(yī)保支付意愿,作為該通用名藥品的準(zhǔn)入門檻;
參與申報(bào)的企業(yè)分別報(bào)價(jià),只要有1家企業(yè)報(bào)價(jià)不高于醫(yī)保支付意愿,則該通用名藥品即可納入醫(yī)保乙類目錄,否則該通用名藥品不納入;
競價(jià)藥品納入醫(yī)保目錄的支付標(biāo)準(zhǔn)取各企業(yè)報(bào)價(jià)中的最低報(bào)價(jià)。
這意味著,對(duì)于“非獨(dú)家藥品”而言,無論是在資料申報(bào)環(huán)節(jié),還是現(xiàn)場競價(jià)環(huán)節(jié),企業(yè)都存在被競爭對(duì)手拉低中選價(jià)格的風(fēng)險(xiǎn)。不過,綜合考慮供應(yīng)保障和鼓勵(lì)創(chuàng)新,醫(yī)保談判競價(jià)的核心導(dǎo)向依然是堅(jiān)持“價(jià)格合理”,政策方面顯示,如果企業(yè)報(bào)價(jià)低于醫(yī)保支付意愿的70%,將以醫(yī)保支付意愿的70%兜底。
此時(shí)此刻,新一輪醫(yī)保談判大幕已經(jīng)拉開。去年醫(yī)保藥品目錄調(diào)整共對(duì)117個(gè)藥品進(jìn)行了談判,談判成功94個(gè),總體成功率80.34%??芍^成績斐然;今年醫(yī)保談判,將有哪些重磅品種入圍并最終實(shí)現(xiàn)“以價(jià)換量”,顯然值得市場期待。
02、PD-1產(chǎn)品仍受關(guān)注 國談CAR-T再添一員?
據(jù)行業(yè)數(shù)據(jù)梳理,目前潛在國家醫(yī)保談判品種超過250個(gè),其中2021年通過形式審查、未進(jìn)入醫(yī)保的新通用名藥品超過90個(gè),2022年獲批的新通用名藥物約60個(gè),以及醫(yī)保目錄內(nèi)獲批新適應(yīng)癥藥品和到期續(xù)約品種百余個(gè)。
今年可能參與談判的品種中看點(diǎn)頗多,恒瑞有3個(gè)新產(chǎn)品沖擊醫(yī)保談判,百濟(jì)也有 2 款創(chuàng)新藥待談,國產(chǎn)各大PD-1適應(yīng)癥進(jìn)一步增加,復(fù)星凱特和藥明巨諾的 CAR-T能否進(jìn)入談判也備受關(guān)注。
作為腫瘤免疫治療的“基石”,國產(chǎn)PD-1/L1領(lǐng)域一直是腫瘤市場競爭的“紅海”,也是每年醫(yī)保談判的重要看點(diǎn)。
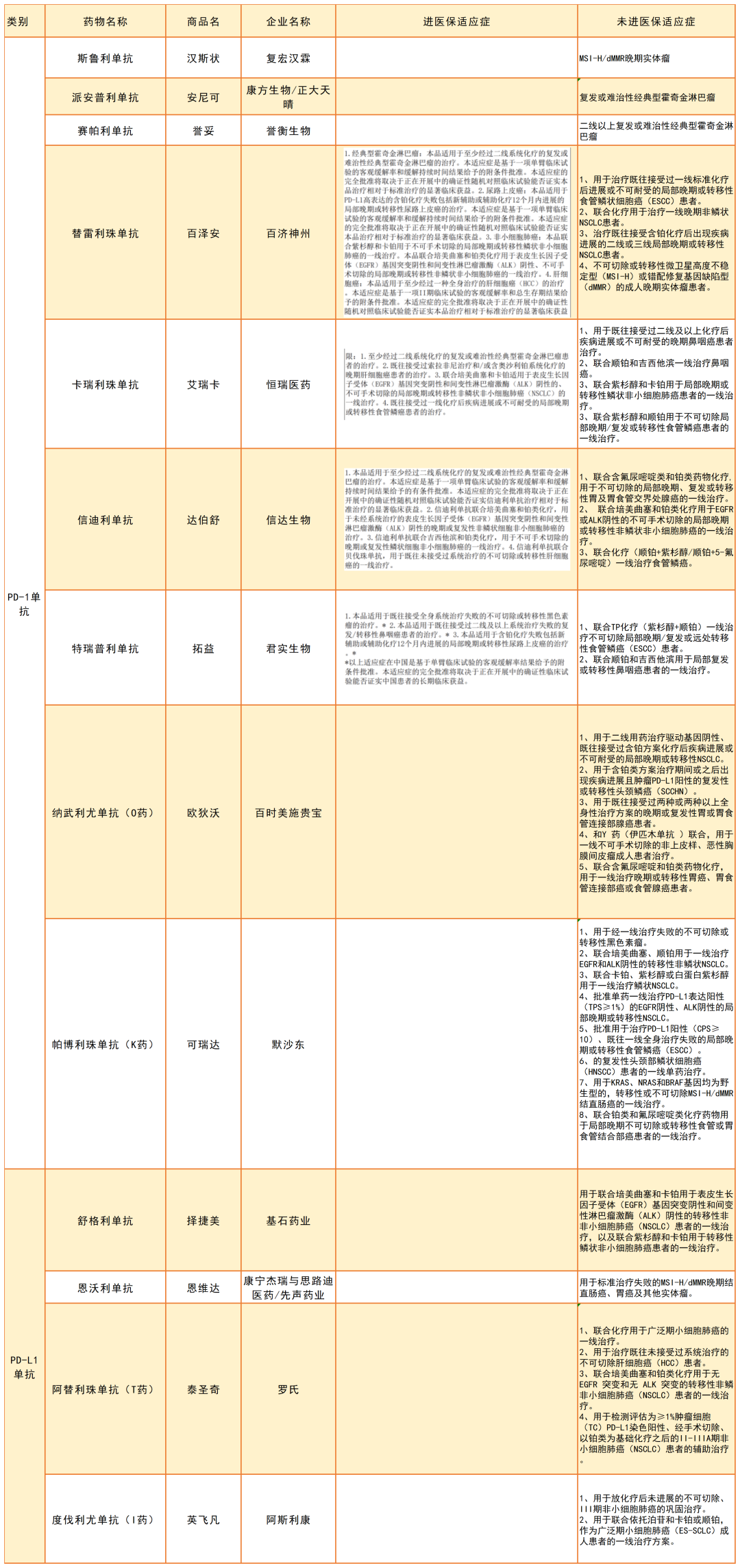
作為腫瘤領(lǐng)域重磅用藥,PD-1因廣闊的市場前景備受期待,又因藥企扎堆布局“內(nèi)卷”,歷次醫(yī)保談判中,PD-1的價(jià)格一降再降被推到風(fēng)口浪尖。
3月4日,復(fù)宏漢霖的PD-1單抗斯魯利單抗獲批上市,用于經(jīng)過標(biāo)準(zhǔn)治療失敗的、不可切除或轉(zhuǎn)移性高度微衛(wèi)星不穩(wěn)定型實(shí)體瘤。自此之后,目前國內(nèi)上市PD-1/PD-L1已經(jīng)高達(dá)13種,競爭壓力不斷增大。
6月23日,信達(dá)生物 PD-1 信迪利單抗新適應(yīng)癥上市申請(qǐng)已獲得批準(zhǔn)。官方信息顯示,本次信迪利單抗獲批的新適應(yīng)癥為:聯(lián)合含氟尿嘧啶類和鉑類藥物化療一線治療不可切除的局部晚期、復(fù)發(fā)性或轉(zhuǎn)移性胃或胃食管交界處腺癌(G/GEJ)。成功搭上本次醫(yī)保談判的“末班車”。
去年6月30日之后,四大國產(chǎn)PD-1已有8項(xiàng)新適應(yīng)癥獲批,2022年,在國產(chǎn)各大PD-1適應(yīng)癥進(jìn)一步增加的情況下,醫(yī)保談判似乎更加備受關(guān)注。
除PD-1外,一些高價(jià)藥在醫(yī)保談判中的表現(xiàn)也值得業(yè)界期待。去年,復(fù)星凱特的CAR-T療法阿基侖賽注射液、藥明巨諾的 CAR-T 療法瑞基奧侖賽注射液先后獲批上市,單價(jià)分別是120萬元和129萬元。
隨后,阿基侖賽出現(xiàn)在2021年醫(yī)保談判的《通過形式審查藥品名單》引發(fā)熱議;不過,據(jù)報(bào)道,在最后的醫(yī)保談判環(huán)節(jié),復(fù)星凱特并未現(xiàn)身醫(yī)保談判現(xiàn)場。
專家分析認(rèn)為,目前獲批的CAR-T產(chǎn)品均為后線治療,這意味著在接受CAR-T治療前,患者必須先經(jīng)過兩種或以上的其他療法治療;因此,雖然CAR-T的臨床療效在血液腫瘤治療中已經(jīng)得到充分驗(yàn)證,但應(yīng)用場景依然存在局限。“去年,復(fù)星凱特的阿基侖賽注射液通過了資格審查,可以參加醫(yī)保談判,但由于沒有競品,降價(jià)和談判的實(shí)際市場意義并不大。”

