近日,復(fù)星醫(yī)藥的創(chuàng)新藥斯魯利單抗注射液在國(guó)內(nèi)外均取得新進(jìn)展。作為醫(yī)藥龍頭企業(yè),近年來復(fù)星醫(yī)藥持續(xù)閃耀在全球市場(chǎng)上。在創(chuàng)新藥方面,復(fù)星醫(yī)藥具有豐富的產(chǎn)品管線,拿下國(guó)內(nèi)首款CAR-T產(chǎn)品,PD-1實(shí)現(xiàn)“泛癌種”精準(zhǔn)治療差異化競(jìng)爭(zhēng),此外有24款1類新藥正在路途中;在仿制藥方面,復(fù)星醫(yī)藥20個(gè)首仿品種獲批,過評(píng)品種達(dá)54個(gè),其中19個(gè)為首家過評(píng)。不僅如此,復(fù)星醫(yī)藥將目標(biāo)拓寬至整個(gè)醫(yī)療生態(tài)領(lǐng)域,目前在新冠、醫(yī)美以及高端醫(yī)療器械等多個(gè)風(fēng)口賽道上“比翼齊飛”......
3大產(chǎn)品過10億大關(guān),24款1類新藥可期
3月23日,復(fù)星醫(yī)藥發(fā)布2021年業(yè)績(jī)報(bào)告,公司全年實(shí)現(xiàn)營(yíng)業(yè)收入390.05億元,同比增長(zhǎng)28.70%,其中制藥業(yè)務(wù)營(yíng)收達(dá)289.04億元,同比增長(zhǎng)32.10% 。銷售額過億的制劑單品或系列共44個(gè),較去年凈增加5個(gè)。從細(xì)分產(chǎn)品來看,mRNA新冠疫苗、利妥昔單抗注射液以及肝素系列制劑相關(guān)產(chǎn)品銷售規(guī)模已超過10億元。其中,國(guó)內(nèi)首個(gè)生物類似藥利妥昔單抗注射液全年收入16.9億元,同比增長(zhǎng)125.33%;2020年下半年上市的注射用曲妥珠單抗、馬來酸阿伐曲泊帕片全年收入分別為9.3億元和4.26億元。
在備受矚目的創(chuàng)新藥板塊,復(fù)星醫(yī)藥持續(xù)發(fā)揮行業(yè)龍頭的優(yōu)勢(shì),資金投入上可謂毫不吝嗇,力度僅次于百濟(jì)神州、恒瑞兩家企業(yè)。據(jù)企業(yè)年報(bào)顯示,復(fù)星醫(yī)藥2021年制藥業(yè)務(wù)研發(fā)投入為44.86億元,同比增長(zhǎng)22.23%。
目前復(fù)星醫(yī)藥已有多款創(chuàng)新藥獲批上市,包括國(guó)內(nèi)首款CART產(chǎn)品阿基侖賽注射液、斯魯利單抗注射液等。值得一提的是,斯魯利單抗注射液實(shí)現(xiàn)了PD-1“泛癌種”精準(zhǔn)治療差異化競(jìng)爭(zhēng),此外,該藥針對(duì)小細(xì)胞肺癌(SCLC)獲得了美國(guó)FDA孤兒藥資格認(rèn)定,在國(guó)內(nèi)針對(duì)SCLC的上市申請(qǐng)也獲受理,未來有望成為全球首個(gè)一線治療SCLC的抗PD-1單抗。
復(fù)星醫(yī)藥已上市部分創(chuàng)新藥
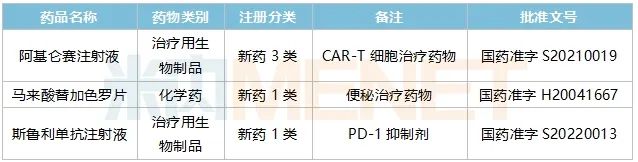
來源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
據(jù)企業(yè)年報(bào)顯示,目前復(fù)星醫(yī)藥擁有60多個(gè)創(chuàng)新藥項(xiàng)目,1類新藥項(xiàng)目超30個(gè),不過大多處于臨床階段。在研創(chuàng)新藥涵蓋腫瘤及免疫調(diào)節(jié)、代謝及消化系統(tǒng)、中樞神經(jīng)系統(tǒng)等治療領(lǐng)域。在靶點(diǎn)分布上,復(fù)星醫(yī)藥也布局PD-1/L1、CD19、c-Met、TOP1、EGFR等多個(gè)熱門靶點(diǎn),并且在RNA、基因治療以及雙抗等前沿療法上也不甘落伍。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前復(fù)星醫(yī)藥在國(guó)內(nèi)處于臨床階段的自研創(chuàng)新藥超過25款(不含已上市新藥開發(fā)新適應(yīng)癥),其中24款為1類新藥,丁二酸復(fù)瑞替尼膠囊、FCN-437c膠囊、重組抗VEGF人源化單克隆抗體眼用注射液3款已進(jìn)入臨床Ⅲ期階段,F(xiàn)CN-159片、HLX208片、注射用FN-1501、HLX07單抗注射液等6款已進(jìn)入臨床Ⅱ期階段。此外,在2022年初,復(fù)星醫(yī)藥的HLX35(4-1BB/EGFR)、HLX301(PD-L1/TIGIT)等雙抗類藥物已在國(guó)內(nèi)和澳大利亞等國(guó)家地區(qū)獲得臨床試驗(yàn)批準(zhǔn),不久后將展開Ⅰ期臨床。
復(fù)星醫(yī)藥在研1類新藥(部分)
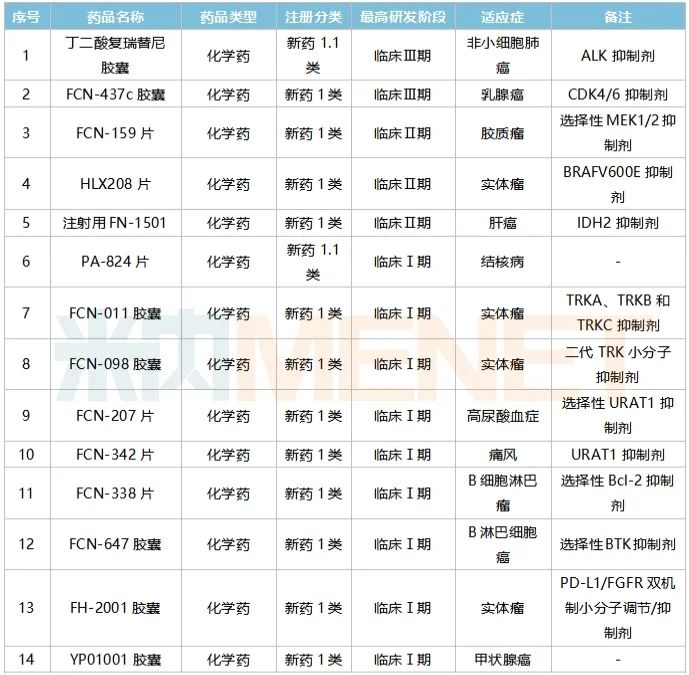
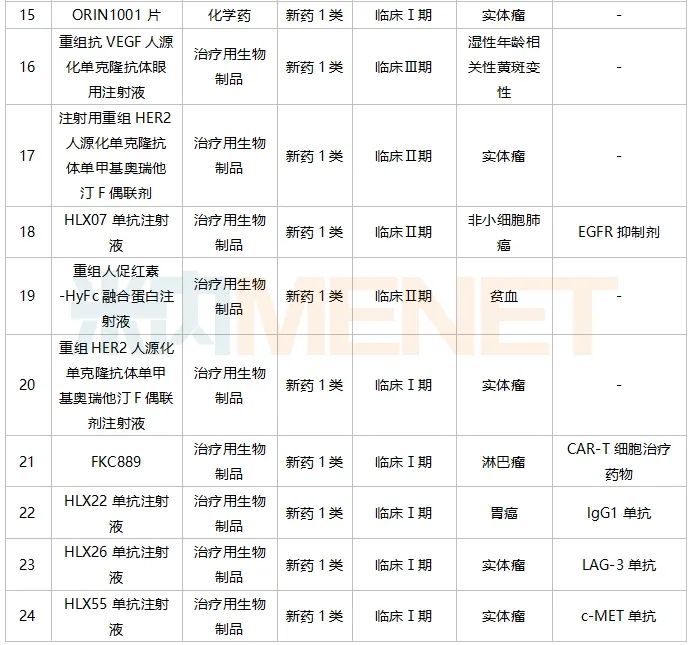
來源:米內(nèi)網(wǎng)中國(guó)藥品臨床試驗(yàn)公示庫(kù)
全球市場(chǎng)增勢(shì)斐然,mRNA疫苗“競(jìng)速”上市
國(guó)際化一直為復(fù)星醫(yī)藥的布局重點(diǎn),在戰(zhàn)略方向上,復(fù)星醫(yī)藥將自身定位為“國(guó)際化醫(yī)藥健康產(chǎn)業(yè)集團(tuán)”,企業(yè)也曾表示未來海外業(yè)務(wù)市場(chǎng)占比要提升至一半左右。據(jù)企業(yè)年報(bào)顯示,2021年復(fù)星醫(yī)藥海外收入達(dá)到135.99億元,同比增長(zhǎng)66.08%,收入占比由去年的27.02%增長(zhǎng)至34.86%。目前,復(fù)星醫(yī)藥與BioNtech、Polyphor、Getz制藥、吉利德等多家海外企業(yè)展開合作,通過并購(gòu)、引進(jìn)等多種方式豐富企業(yè)創(chuàng)新藥產(chǎn)品管線。
在許可引進(jìn)方面,復(fù)星醫(yī)藥已引進(jìn)10余項(xiàng)產(chǎn)品,其中阿基侖賽注射液與mRNA新冠疫苗兩款產(chǎn)品備受市場(chǎng)關(guān)注。已上市的阿基侖賽注射液由復(fù)星醫(yī)藥與吉利德(Kite)合營(yíng)的公司復(fù)星凱特所研發(fā),為國(guó)內(nèi)首款、全球第六款獲批上市的CAR-T細(xì)胞治療藥物。此前業(yè)內(nèi)透露,阿基侖賽注射液的價(jià)格達(dá)到120萬元一針。如果按照這個(gè)價(jià)格來估算,從去年6月獲批到2021年底,阿基侖賽注射液帶來了至少過億的收入。但是,該藥在2021年醫(yī)保談判中無緣醫(yī)保,高昂的價(jià)格使得多數(shù)患者望而止卻步,目前在市場(chǎng)普及推動(dòng)方面仍遭受不少阻礙。
與BioNtech合作的mRNA新冠疫苗(BNT162b2)目前已率先投入在港澳臺(tái)等地區(qū)使用。目前,該疫苗在大陸地區(qū)正處于臨床Ⅱ期階段,在內(nèi)地的上市申請(qǐng)也在審評(píng)審批中。業(yè)內(nèi)人士表示,只需要在國(guó)內(nèi)完成Ⅱ期橋接臨床試驗(yàn),就能與國(guó)外所獲得的Ⅲ期臨床試驗(yàn)數(shù)據(jù)一起提交給藥監(jiān)局審批上市,有望沖刺國(guó)內(nèi)首款。除此之外,與之競(jìng)速上市的國(guó)產(chǎn)候選mRNA新冠疫苗還包括艾博生物的ARCoV(臨床Ⅲ期)、麗凡達(dá)的LVRNA009(臨床Ⅱ期)等。
在海外商業(yè)化方面,復(fù)星醫(yī)藥依托藥友制藥、桂林南藥、萬邦醫(yī)藥等子公司已有國(guó)際化生產(chǎn)水平和質(zhì)量體系認(rèn)證,為國(guó)內(nèi)生產(chǎn)的制劑產(chǎn)品出海打下基礎(chǔ)。據(jù)企業(yè)介紹,復(fù)星醫(yī)藥子公司Tridem Pharma在非洲的首個(gè)區(qū)域性藥品分銷中心科特迪瓦分銷中心正式投入運(yùn)營(yíng),業(yè)務(wù)在南蘇丹取得實(shí)質(zhì)性銷售突破;印度控股子公司Gland Pharma共計(jì)13個(gè)仿制藥產(chǎn)品獲得美國(guó)FDA上市批準(zhǔn)。此外,在2022年初,復(fù)星醫(yī)藥通過WHO-PQ的抗瘧系列產(chǎn)品總數(shù)已增至30個(gè),其中包括26個(gè)制劑產(chǎn)品和4個(gè)原料藥產(chǎn)品,成為全球通過該認(rèn)證數(shù)量最多的抗瘧藥生產(chǎn)企業(yè)。
20個(gè)品種拿下首仿,拓展“風(fēng)口”迎戰(zhàn)集采
從仿制藥情況來看,據(jù)不完全統(tǒng)計(jì),復(fù)星醫(yī)藥首仿品種已有20個(gè),其中以全身抗感染類藥物制劑居多(10個(gè)),哌拉西林舒巴坦、頭孢哌酮他唑巴坦、比卡魯胺等品種在2020年中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端銷售規(guī)模分別超過20億元、15億元、15億元。
復(fù)星醫(yī)藥已獲批首仿品種(部分)
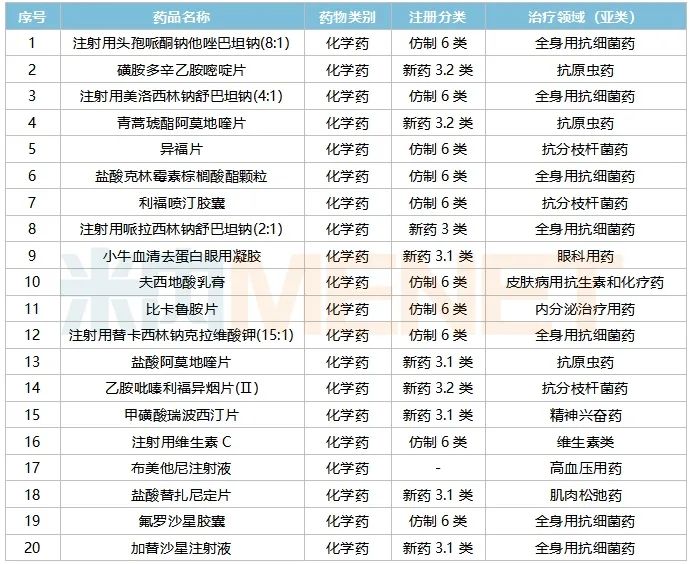
來源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
從過評(píng)情況來看,目前復(fù)星醫(yī)藥已有54個(gè)品種過評(píng),其中19個(gè)為首家過評(píng),丙硫氧嘧啶片、鹽酸阿米替林片兩個(gè)品種為獨(dú)家過評(píng)。
復(fù)星醫(yī)藥首家過評(píng)品種
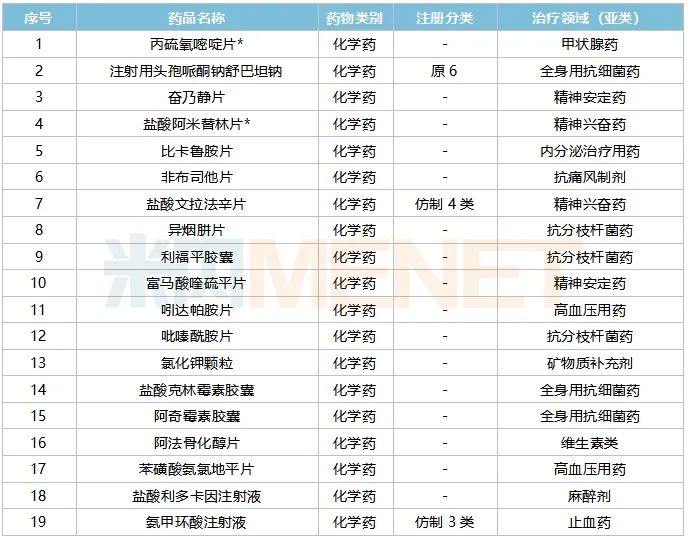
來源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
從集采情況來看,復(fù)星醫(yī)藥已有共有23個(gè)過評(píng)產(chǎn)品(21個(gè)通用名藥品)納入到前6批集采,包括苯磺酸氨氯地平片、鹽酸克林霉素膠囊、鹽酸美金剛片、甲苯磺酸索拉非尼片、吡嗪酰胺片等。不過,在即將開展的第七批集采中,復(fù)星醫(yī)藥目前尚未有產(chǎn)品納入新集采范圍內(nèi)。
復(fù)星醫(yī)藥前6批集采中選產(chǎn)品
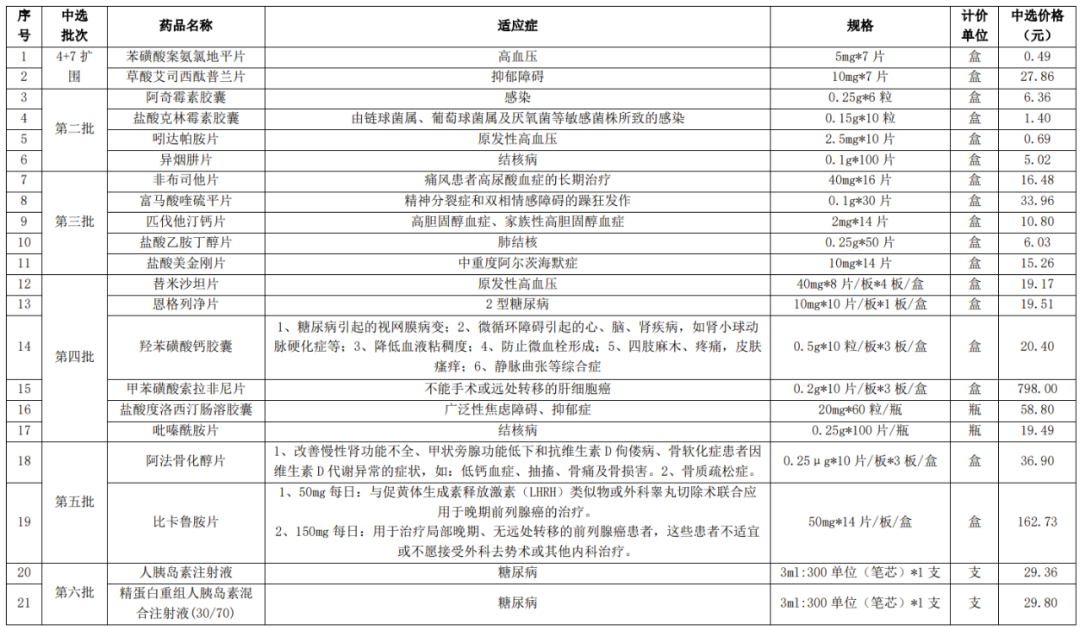
來源:企業(yè)年報(bào)
面對(duì)集采,復(fù)星醫(yī)藥的眼光并未局限在醫(yī)藥領(lǐng)域,在體外診斷、醫(yī)美、高端醫(yī)療器械等醫(yī)療大健康“風(fēng)口”賽道的尖端,均出現(xiàn)復(fù)星醫(yī)藥的身影,復(fù)銳醫(yī)療、復(fù)星診斷等醫(yī)療器械業(yè)務(wù)已覆蓋全球十多個(gè)國(guó)家地區(qū)。例如,在目前如火如荼的體外診斷賽道上,復(fù)星醫(yī)藥涵蓋體外診斷賽道分析儀以及診斷試劑上下游兩大產(chǎn)業(yè)鏈,并擁有豐富的產(chǎn)品管線。米內(nèi)網(wǎng)數(shù)據(jù)顯示,截至2022年3月,復(fù)星醫(yī)藥擁有醫(yī)療器械注冊(cè)批文數(shù)274個(gè),主要為體外診斷試劑,其中3類批文36個(gè)。此外,在高端醫(yī)療器械領(lǐng)域,復(fù)星醫(yī)藥與直覺外科聯(lián)營(yíng)成立直觀復(fù)星公司,拿下了龍頭產(chǎn)品“達(dá)芬奇”手術(shù)機(jī)器人的經(jīng)銷權(quán)收益。在此之前,“達(dá)芬奇”手術(shù)機(jī)器人項(xiàng)目已在上海等地區(qū)納入醫(yī)保,隨著項(xiàng)目普及,未來將會(huì)進(jìn)一步為企業(yè)提供業(yè)績(jī)?cè)隽俊?/div>
資料來源:米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)、企業(yè)年報(bào)
注:統(tǒng)計(jì)截至4月13日,如有疏漏,歡迎指正!



