廣東11省聯(lián)盟276個(gè)藥品集采正式開(kāi)啟,其中血液制品5個(gè),獨(dú)家品種58個(gè)。集采工作將分階段實(shí)施。此次可查看第一批符合申報(bào)條件的企業(yè)分組及報(bào)量情況,涉及579家企業(yè)、1613個(gè)品規(guī),首年預(yù)采購(gòu)量達(dá)154.77億(片/粒/袋/支)。查看時(shí)間即日起至2月25日17:30時(shí)止。
2月23日,廣東省藥品交易中心發(fā)布《關(guān)于查看廣東聯(lián)盟雙氯芬酸等藥品集中帶量采購(gòu)(第一批)報(bào)名產(chǎn)品相關(guān)信息的通知》,第一批共有579家企業(yè)、1613個(gè)品規(guī)符合申報(bào)條件。
《通知》同步公開(kāi)了第一批A/B采購(gòu)單聯(lián)盟地區(qū)公立醫(yī)療機(jī)構(gòu)報(bào)量情況(具體見(jiàn)文末附表)。其中非獨(dú)家品種同組折算為代表規(guī)格的采購(gòu)期首年預(yù)采購(gòu)量150.82億(片/粒/袋/支),獨(dú)家品種折算為代表規(guī)格的采購(gòu)期首年預(yù)采購(gòu)量為3.95億(片/粒/袋/支)。
報(bào)名企業(yè)的申報(bào)品種數(shù)量也可看出企業(yè)的品種結(jié)構(gòu)和規(guī)模。其中排名前列的依次為:瑞陽(yáng)制藥有30個(gè)品規(guī)、羅欣23個(gè)、白云山天心22個(gè)、雙鷺21個(gè)。
第一批報(bào)名品種數(shù)量10個(gè)及以上品規(guī)的企業(yè),如下表所示:
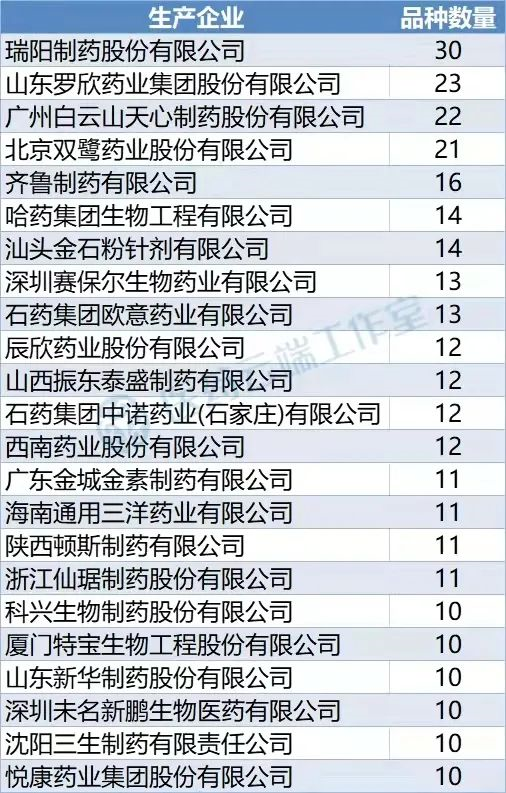
此外,第二批有2602個(gè)品規(guī)、208家企業(yè)符合申報(bào)條件,信息查看等工作開(kāi)展時(shí)間將另行公告。
查看時(shí)間即日起至2月25日17:30時(shí)止。
《通知》明確最低價(jià)格是采集到的截止至2021年12月1日(含)各?。ò◤V東、山西、江西、河南、廣西、海南、貴州、青海、寧夏、新疆、新疆生產(chǎn)建設(shè)兵團(tuán))的最低價(jià)格(指省級(jí)掛網(wǎng)價(jià)格或省級(jí)中標(biāo)價(jià)格)。價(jià)格申報(bào)品規(guī)的最低價(jià)格與基準(zhǔn)品規(guī)的最低價(jià)格就低差比,其他報(bào)名品規(guī)的最低價(jià)格與價(jià)格申報(bào)品規(guī)的最低價(jià)格應(yīng)符合差比。
帶量最低價(jià)格是采集到的截止至目前全國(guó)省級(jí)帶量采購(gòu)的最低中選價(jià)格。
《通知》要求相關(guān)企業(yè)認(rèn)真查看核對(duì)本企業(yè)相關(guān)產(chǎn)品的價(jià)格信息,如發(fā)現(xiàn)存在未申報(bào)、漏報(bào)價(jià)格的,請(qǐng)?jiān)谝?guī)定時(shí)間內(nèi)如實(shí)申報(bào),除上述要求的材料外,還須提供所申報(bào)價(jià)格為上述各?。▍^(qū))截止至2021年12月1日(含)的最低價(jià)格(或截止至目前全國(guó)省級(jí)帶量采購(gòu)最低中選價(jià)格)的承諾書(shū)。
如存在《采購(gòu)文件》所列“同品種同一競(jìng)爭(zhēng)單元申報(bào)企業(yè)中,企業(yè)負(fù)責(zé)人為同一人或存在直接控股、管理關(guān)系”情形的,請(qǐng)相關(guān)企業(yè)在規(guī)定時(shí)間內(nèi)如實(shí)進(jìn)行申報(bào),申報(bào)內(nèi)容需包括涉及的具體競(jìng)爭(zhēng)單元名稱、同競(jìng)爭(zhēng)單元企業(yè)間具體關(guān)系(企業(yè)負(fù)責(zé)人為同一人/存在直接控股關(guān)系/存在管理關(guān)系)以及相關(guān)證明材料,具體要求及申報(bào)方式見(jiàn)上述“反饋方式及要求”。未在規(guī)定時(shí)間內(nèi)進(jìn)行申報(bào)的,視為企業(yè)承諾不存在上述所列情形。
相關(guān)規(guī)則回顧:
1月19日,廣東省藥品交易中心發(fā)布《廣東聯(lián)盟雙氯芬酸等藥品集中帶量采購(gòu)文件》,明確276個(gè)國(guó)家醫(yī)保目錄內(nèi)用量大、采購(gòu)金額高的化學(xué)藥品和治療用生物制品納入本次集采。
其中國(guó)家醫(yī)保目錄外的藥品、國(guó)家已集采未到期醫(yī)保目錄的劑型或規(guī)格、國(guó)家醫(yī)保談判藥品、國(guó)家實(shí)行特殊管理的藥品、通過(guò)(含視同通過(guò),下同)一致性評(píng)價(jià)的仿制藥(截至2021年 11月4日)對(duì)應(yīng)的劑型,不列入本次集采范圍。
采購(gòu)周期和采購(gòu)協(xié)議
原則上不超過(guò)兩年,自中選/備選結(jié)果實(shí)際執(zhí)行日起計(jì)算,首年采購(gòu)期滿后,可續(xù)簽一年。具體執(zhí)行時(shí)間和采購(gòu)周期由聯(lián)盟地區(qū)各省自行確定。
在采購(gòu)周期內(nèi)采購(gòu)協(xié)議每年一簽。第二年續(xù)簽采購(gòu)協(xié)議時(shí)重新報(bào)量,第二年協(xié)議采購(gòu)量原則上不少于該中選/備選產(chǎn)品首年協(xié)議采購(gòu)量。
采購(gòu)周期首年內(nèi)醫(yī)療機(jī)構(gòu)若提前完成當(dāng)年協(xié)議采購(gòu)量,超出協(xié)議采購(gòu)量的部分,優(yōu)先采購(gòu)中選/備選產(chǎn)品,中選/備選企業(yè)按本采購(gòu)文件規(guī)定情形對(duì)應(yīng)的中選/備選價(jià)格進(jìn)行供應(yīng),直至采購(gòu)周期屆滿。
在采購(gòu)周期執(zhí)行過(guò)程中,如國(guó)采的藥品與本次廣東聯(lián)盟集采的藥品存在重復(fù)的,按國(guó)家中選結(jié)果執(zhí)行,并重新簽訂購(gòu)銷合同。
采購(gòu)周期內(nèi),在完成協(xié)議采購(gòu)量后,公立醫(yī)療機(jī)構(gòu)(含未報(bào)量的公立醫(yī)療機(jī)構(gòu))優(yōu)先采購(gòu)使用中選產(chǎn)品,中選/備選產(chǎn)品使用按照不低于增量的70%比例繼續(xù)帶量采購(gòu),未獲得增量使用的備選產(chǎn)品的實(shí)際采購(gòu)量不超過(guò)對(duì)應(yīng)公立醫(yī)療機(jī)構(gòu)填報(bào)的采購(gòu)量乘以首年約定采購(gòu)比例。
醫(yī)保定點(diǎn)社會(huì)辦醫(yī)療機(jī)構(gòu)和定點(diǎn)藥店的采購(gòu)量由供需雙方按采購(gòu)協(xié)議的約定執(zhí)行。
企業(yè)梯極報(bào)價(jià),最低價(jià)要求:
1、最低價(jià)格是指截止至2021年12月1日(含)各省(包括廣東、山西、江西、河南、廣西、海南、貴州、青海、寧夏、新疆和新疆生產(chǎn)建設(shè)兵團(tuán))的最低價(jià)格(指省級(jí)掛網(wǎng)價(jià)格或省級(jí)中標(biāo)價(jià)格)。最低日均費(fèi)用=最低價(jià)格×日均用量。
血液制品、非獨(dú)家藥品和獨(dú)家藥品,以聯(lián)盟地區(qū)公立醫(yī)療機(jī)構(gòu)填報(bào)的同企業(yè)同品種首年預(yù)采購(gòu)量(指片/粒/袋/支等)最大的品規(guī)為基準(zhǔn)品規(guī),申報(bào)品規(guī)的最低價(jià)格/最低日均費(fèi)用與基準(zhǔn)品規(guī)的最低價(jià)格/最低日均費(fèi)用就低差比。
2、葡萄糖/氯化鈉/葡萄糖氯化鈉注射劑同企業(yè)同品種同組同裝量不同濃度不區(qū)分價(jià)格,取低值作為最低價(jià)格。同企業(yè)同品種同組10ml(含)以下不同含量的小容量注射液不區(qū)分價(jià)格,取10ml(含)以下不同含量?jī)r(jià)格最低的作為最低價(jià)格。
3、濃氯化鈉注射劑、生理氯化鈉沖洗劑和腹膜透析液注射劑,同企業(yè)同品種同組同裝量不同濃度不區(qū)分價(jià)格,取低值作為最低價(jià)格。同組不同裝量按照每10ml以上的,每增(減)10ml,加(減)0.05元的差比價(jià)計(jì)算價(jià)格。同企業(yè)同品種同組10ml(含)以下不同含量的小容量注射液不區(qū)分價(jià)格,取10ml(含)以下不同含量?jī)r(jià)格最低的作為最低價(jià)格。
4、血液制品、非獨(dú)家藥品(除濃氯化鈉注射劑、生理氯化鈉沖洗劑和腹膜透析液注射劑外)和獨(dú)家藥品中,同組注射劑中的普通粉針、凍干粉針、溶媒結(jié)晶粉針不區(qū)分劑型差比價(jià);若注射劑中劑型差比價(jià)與含量差比價(jià)混合計(jì)算出現(xiàn)負(fù)值時(shí),僅按含量差比價(jià)計(jì)算;同企業(yè)同品種小容量注射液10ml(含)以下同含量的,取同含量不同裝量?jī)r(jià)格最低的作為最低價(jià)格。
5.生物制品小容量注射液采用預(yù)充式注射器包裝單次劑量藥品的,以同品規(guī)普通小容量注射液的價(jià)格為基礎(chǔ),每支增加3元;不同規(guī)格的預(yù)充式,以同企業(yè)普通小容量注射液的價(jià)格為基礎(chǔ),折算至相應(yīng)規(guī)格的價(jià)格后,每支增加3元(預(yù)充式以國(guó)家藥監(jiān)部門(mén)頒發(fā)的批件為準(zhǔn))。
6.同企業(yè)同品種同劑型同規(guī)格含糖和不含糖不區(qū)分價(jià)格,取同規(guī)格的低值作為最低價(jià)格。



