12月22日,恒瑞醫(yī)藥2款1類新藥的臨床申請獲得CDE承辦受理,此外首家以新注冊分類提交10%脂肪乳(OO)/5.5%氨基酸(15)/葡萄糖(20%)注射液上市申請。米內(nèi)網(wǎng)數(shù)據(jù)顯示,近1周,恒瑞醫(yī)藥有7款新藥(6款為1類新藥)申報(bào)臨床。
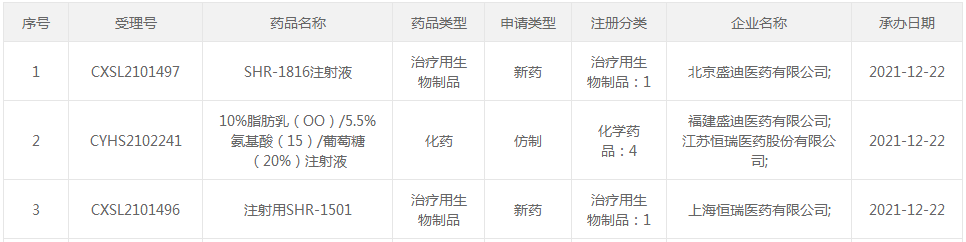
來源:CDE官網(wǎng)
12月22日,恒瑞醫(yī)藥2款1類新藥的臨床申請、1款4類仿制藥的上市申請獲得CDE承辦受理。目前國內(nèi)僅百特的10%脂肪乳(OO)/5.5%氨基酸(15)/葡萄糖(20%)注射液(商品名克林玫)在售,恒瑞醫(yī)藥首家以新分類報(bào)產(chǎn);2款1類新藥中,SHR-1816注射液首次在國內(nèi)申報(bào)臨床。
創(chuàng)新藥和首仿是恒瑞醫(yī)藥聚焦的重點(diǎn),米內(nèi)網(wǎng)數(shù)據(jù)顯示,近1周(12月17-23日),恒瑞醫(yī)藥有7款新藥(含非首次申報(bào))、1款仿制藥提交臨床/上市申請,其中6款為1類新藥。
12月17-23日恒瑞醫(yī)藥申請上市/臨床的品種
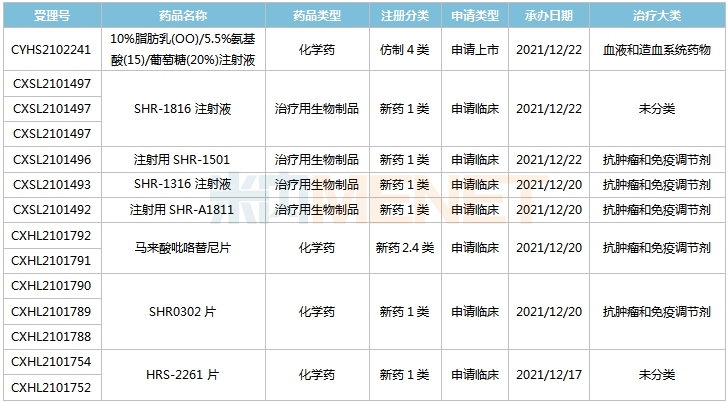
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評(píng)數(shù)據(jù)庫
6款1類新藥中,SHR-1816注射液、HRS-2261片首次在國內(nèi)提交臨床申請。
非首次申報(bào)的新藥中,SHR0302片是一款JAK1激酶選擇性抑制劑,活動(dòng)性類風(fēng)濕關(guān)節(jié)炎、特應(yīng)性皮炎等適應(yīng)癥在開展III期臨床;SHR-1316注射液為PD-L1單抗,廣泛期小細(xì)胞肺癌等適應(yīng)癥已步入III期臨床;注射用SHR-1501是一款白細(xì)胞介素-15(IL-15)融合蛋白,晚期惡性腫瘤適應(yīng)癥在開展I期臨床;注射用SHR-A1811是一款靶向Her2的ADC藥物,晚期非小細(xì)胞肺癌適應(yīng)癥在開展I/II期臨床。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、CDE官網(wǎng)等



