近段時間,“創(chuàng)新藥一哥”恒瑞醫(yī)藥動態(tài)頻發(fā):3款1類新藥殺入新醫(yī)保,SHR8554、SHR8008、SHR8058即將報產(chǎn)......米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前恒瑞有108款創(chuàng)新藥(81款1類新藥)處于申請臨床及以上階段,其中11款(9款1類新藥)已/即將報產(chǎn),13款(9款1類新藥)處于III期(含II/III期)關(guān)鍵臨床,此外“license-in”不斷提速;仿制藥方面,47個品種過評(22個為首家),16個沖刺首仿(7個獨家報產(chǎn))。
5款創(chuàng)新藥大賣超100億,3款1類新藥殺入新醫(yī)保
經(jīng)過多年布局,恒瑞醫(yī)藥創(chuàng)新藥步入收獲期。今年以來,公司有3款新藥獲批上市,含1類新藥海曲泊帕乙醇胺片(TPO-R激動劑);此外,多款已上市1類新藥新適應癥獲批,包括甲苯磺酸瑞馬唑侖、氟唑帕利、卡瑞利珠單抗、阿帕替尼等。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前恒瑞醫(yī)藥有8款創(chuàng)新藥獲批上市,2020年之前獲批的5款創(chuàng)新藥在2020年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構(gòu))及中國城市實體藥店終端合計銷售規(guī)模超過100億元,預計2021年將再創(chuàng)新高。
恒瑞醫(yī)藥已上市創(chuàng)新藥銷售情況
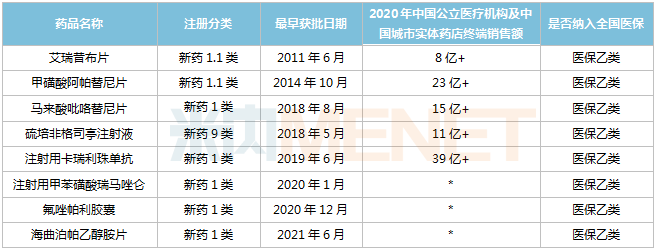
注:低于1億元用*代表
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫
2020年之后獲批的3款1類新藥參與2021年全國醫(yī)保談判,全部成功入選。截至目前,恒瑞醫(yī)藥進入國家醫(yī)保目錄的藥品總數(shù)已達85個,其中包括已獲批上市的8款創(chuàng)新藥。
在12月3日發(fā)布的新版全國醫(yī)保目錄中,恒瑞有9款產(chǎn)品被納入,其中3款1類新藥、1款首仿為首次納入,1款新藥新增適應癥,2款新藥為續(xù)約產(chǎn)品。
恒瑞醫(yī)藥納入新版醫(yī)保的產(chǎn)品
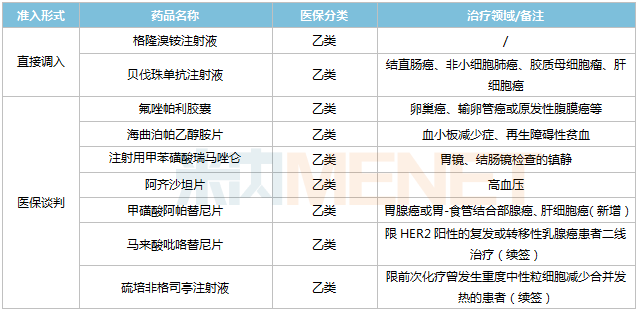
來源:國家醫(yī)保局官網(wǎng)
“license-in”再提速,81款1類新藥霸屏
11月21日,恒瑞醫(yī)藥與基石藥業(yè)的合作引起業(yè)內(nèi)廣泛關(guān)注。恒瑞將以5200萬元首付款、不超過11.85億元的里程碑款引進基石在研抗CTLA-4單抗CS1002注射液,目前國內(nèi)同靶點上市藥物為百時美施貴寶的伊匹木單抗。
CTLA-4與PD-1、PD-L1并稱為腫瘤免疫藥物開發(fā)靶點的“三寶”,是主流腫瘤免疫療法的基礎(chǔ)構(gòu)成部分。此次合作一方面可緩解恒瑞在CTLA-4靶點研發(fā)的落后局面,另一方面也給公司已上市PD-1及在研PD-L1的聯(lián)合用藥鋪路。
今年以來,恒瑞醫(yī)藥公布的合作項目至少有4個,引進的都是同類中進展較快的創(chuàng)新藥(以生物藥為主),如天廣實的MIL62,是首款進入III臨床的國產(chǎn)第三代CD20單抗,國內(nèi)同靶點上市藥物為羅氏的奧妥珠單抗(2020年全球銷售額6.32億瑞士法郎);瓔黎藥業(yè)的YY-20394,是首款提交上市申請的國產(chǎn)PI3kδ抑制劑,國內(nèi)暫無同靶點藥物獲批。
2019年至今恒瑞醫(yī)藥公布的license-in

來源:上市公司公告、米內(nèi)網(wǎng)數(shù)據(jù)庫
從過去悶頭搞自主研發(fā)到接連引進創(chuàng)新藥,從研發(fā)投入全部費用化到研發(fā)投入部分資本化......恒瑞醫(yī)藥正在積極謀變,而不變的是堅持研發(fā)創(chuàng)新與國際化的初心與決心。季報數(shù)據(jù)顯示,2021年前三季度公司研發(fā)投入41.4億元,比去年同期增長23.9%,占營收比重20.5%(去年同期為17.2%)。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,含合作引進的新藥在內(nèi),目前恒瑞醫(yī)藥有108款創(chuàng)新藥(不含已上市新藥開發(fā)新適應癥)處于申請臨床及以上階段,其中有81款為1類新藥。
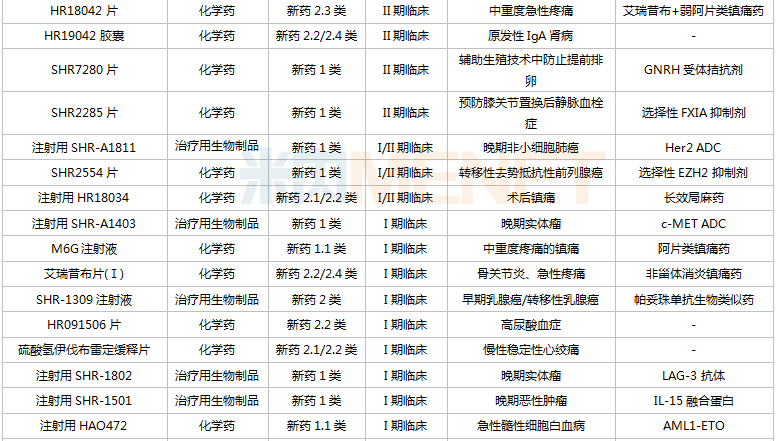
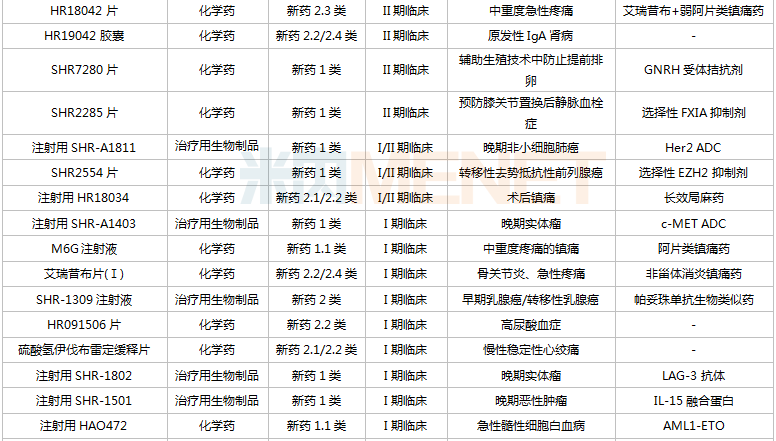
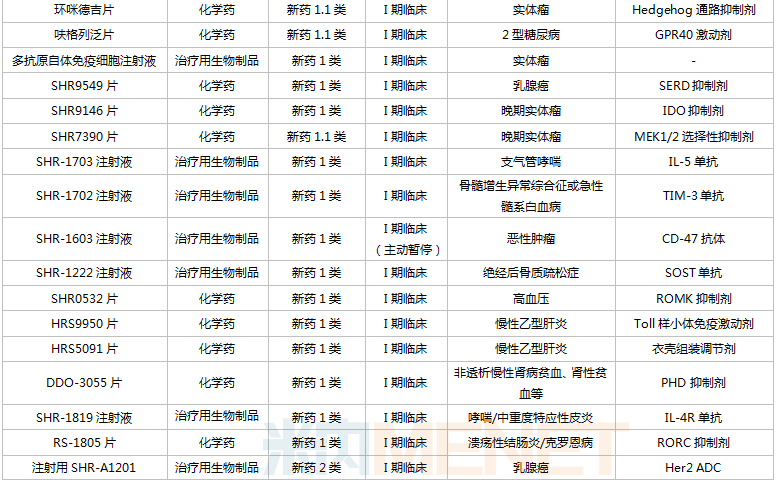
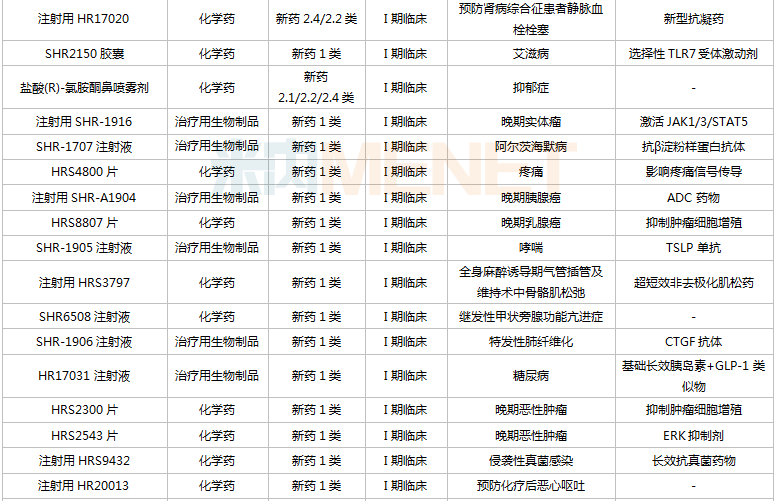
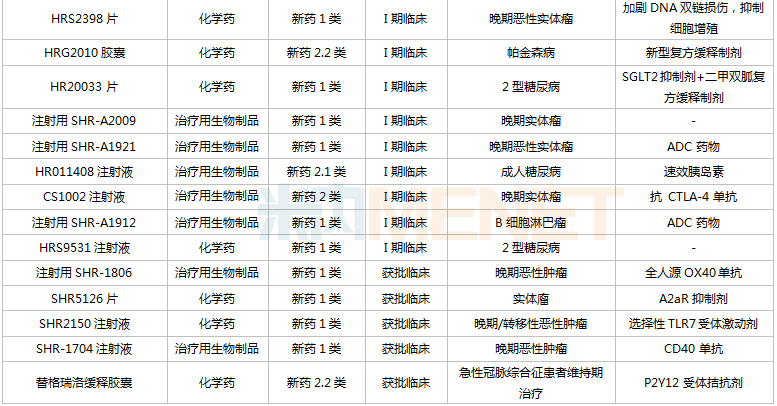
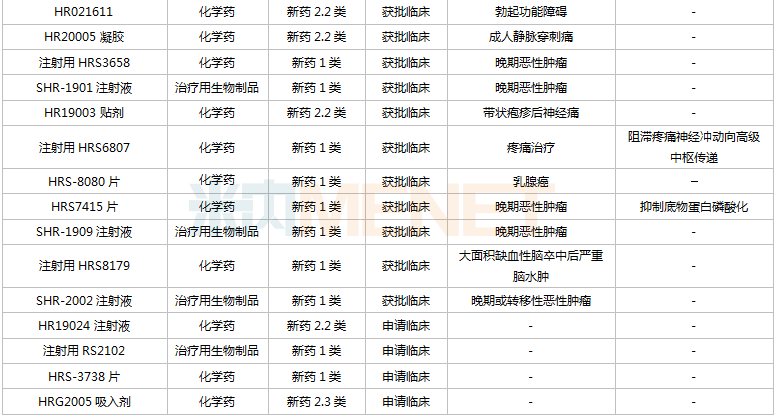
恒瑞醫(yī)藥在研創(chuàng)新藥
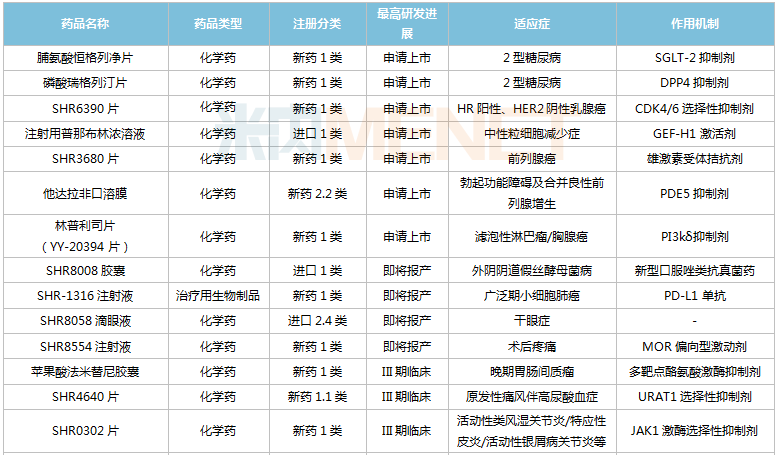
注:帶*為首家過評,**為獨家過評
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
22個品種首家/獨家過評,其中塞來昔布膠囊、格隆溴銨注射液、鹽酸艾司氯胺酮注射液、醋酸阿比特龍片、注射用替莫唑胺、鹽酸右美托咪定氯化鈉注射液、托伐普坦片、他氟前列素滴眼液、麥考酚鈉腸溶片、阿齊沙坦片等品種為首仿+首家過評。
恒瑞醫(yī)藥新分類報產(chǎn)仿制藥中,有16個暫無首仿(含首個劑型)獲批。多個產(chǎn)品在國內(nèi)有其他劑型在售,可見劑型改良是公司重點研發(fā)方向之一。
恒瑞醫(yī)藥新分類報產(chǎn)且暫無首仿獲批的品種
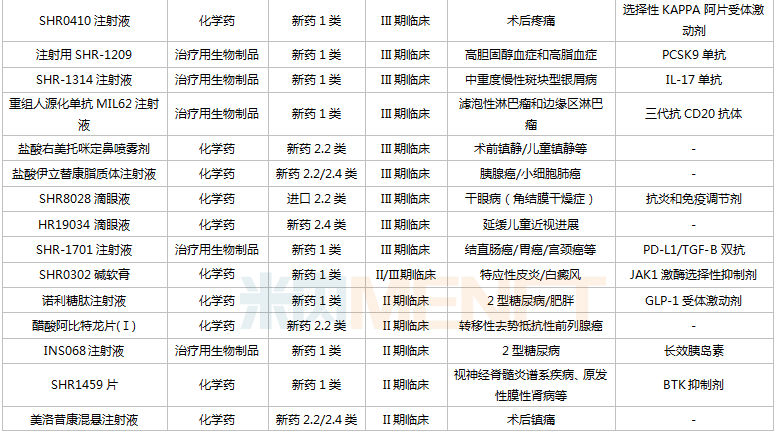

來源:米內(nèi)網(wǎng)中國藥品臨床試驗公示庫
從研發(fā)進展看,11款新藥已/即將申報上市(最高研發(fā)進展,下同),除了他達拉非口溶膜及SHR8058滴眼液,其余9款均為1類新藥;13款新藥步入III期(含II/III期)關(guān)鍵臨床,其中9款為1類新藥。
從治療領(lǐng)域看,108款創(chuàng)新藥涉及十多個治療類別,全方位、多病種、多器官覆蓋,集中在抗腫瘤、神經(jīng)系統(tǒng)(疼痛、抑郁癥、帕金森等)、消化系統(tǒng)(2型糖尿病、止嘔等)等治療領(lǐng)域,其中抗腫瘤藥獨占近“半壁江山”,涵蓋肺癌、乳腺癌、肝癌、胃癌、婦科腫瘤、泌尿腫瘤、血液腫瘤等多個病種。
從治療靶點看,恒瑞醫(yī)藥布局全球熱門靶點和前沿療法,如PD-1/PD-L1、BTK、CDK4/6、JAK等;多個藥物在國內(nèi)外尚無同靶點產(chǎn)品獲批,包括全人源OX40單抗、Toll樣小體免疫激動劑、選擇性FXIA抑制劑、A2aR抑制劑、ROMK抑制劑、LAG-3抗體、TIM-3單抗等;此外公司還積極擁抱新技術(shù),自研ADC藥物,發(fā)力雙抗/多抗,布局基因治療等。
22個品種首家過評,16個品種沖刺首仿
11月13日,恒瑞醫(yī)藥公告稱,公司4類仿制藥他氟前列素滴眼液獲批生產(chǎn),為國內(nèi)首仿。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年至今,公司有12款仿制藥獲批生產(chǎn)并視同過評,其中5款為首仿,包括他氟前列素滴眼液、鹽酸右美托咪定氯化鈉注射液、托伐普坦片、麥考酚鈉腸溶片及阿齊沙坦片。
目前恒瑞醫(yī)藥有47個品種通過或視同通過一致性評價,涵蓋12個治療大類,集中在抗腫瘤和免疫調(diào)節(jié)劑(12個品種)及神經(jīng)系統(tǒng)藥物(9個品種);從劑型分布看,含21款注射劑、4款緩控釋制劑、2款吸入劑、1款滴眼劑等。
恒瑞醫(yī)藥過評情況
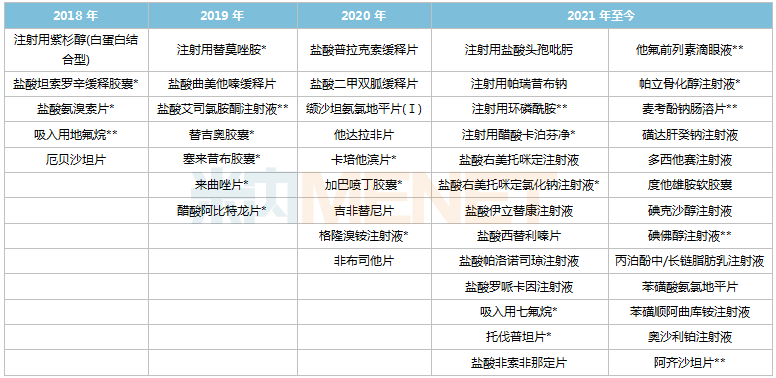
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
2個品種首家/獨家過評,其中塞來昔布膠囊、格隆溴銨注射液、鹽酸艾司氯胺酮注射液、醋酸阿比特龍片、注射用替莫唑胺、鹽酸右美托咪定氯化鈉注射液、托伐普坦片、他氟前列素滴眼液、麥考酚鈉腸溶片、阿齊沙坦片等品種為首仿+首家過評。
恒瑞醫(yī)藥新分類報產(chǎn)仿制藥中,有16個暫無首仿(含首個劑型)獲批。多個產(chǎn)品在國內(nèi)有其他劑型在售,可見劑型改良是公司重點研發(fā)方向之一。
恒瑞醫(yī)藥新分類報產(chǎn)且暫無首仿獲批的品種
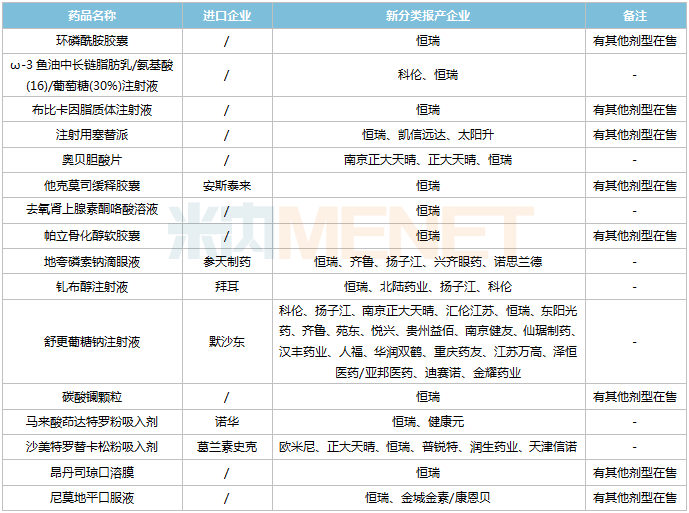
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
7個品種由恒瑞醫(yī)藥獨家以新分類報產(chǎn),涉及脂質(zhì)體(布比卡因脂質(zhì)體注射液)、口溶膜(昂丹司瓊口溶膜)、緩控釋制劑(他克莫司緩釋膠囊)等高端制劑。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、上市公司公告等
注:米內(nèi)網(wǎng)中國城市實體藥店終端競爭格局數(shù)據(jù)庫是覆蓋全國293個地市及以上城市實體藥店(不含縣鄉(xiāng)村實體藥店),對全品類進行連續(xù)監(jiān)測的放大版城市實體藥店數(shù)據(jù)庫。上述銷售額以產(chǎn)品在終端的平均零售價計算。數(shù)據(jù)統(tǒng)計截至12月6日,如有疏漏,歡迎指正!



